作者:中科睿极
浏览量:216

2026-03-09
分享

银屑病作为影响全球 2%-3%人口的慢性炎症性皮肤病,以异常角质形成细胞增殖和免疫细胞浸润为核心特征,现有生物治疗易出现复发、耐药等问题,亟需更安全有效的治疗策略。2026年2月3日,深圳市南山区人民医院陈宏翔教授联合中科睿极首席科学家张智勇教授团队在国际权威免疫学期刊《Frontiers in Immunology》发表题为“Evaluation of 3D biomimetic microcarriers for enhancing therapeutic efficacy of human umbilical cord mesenchymal stem cells in psoriasis treatment(基于3D微载体-生物反应器系统增强hUC-MSCs对银屑病的治疗效果)”的研究论文,创新性地将3D微载体-生物反应器系统应用于人脐带间充质干细胞(hUCMSCs)的培养,显著增强了其对银屑病的治疗效果,为银屑病治疗领域带来新突破!
研究背景
间充质干细胞(MSCs)凭借自我更新、多向分化及免疫调节等特性,在再生医学领域展现出广阔前景,尤其在银屑病等免疫介导疾病的治疗中备受关注。人脐带间充质干细胞(hUCMSCs)更是因来源丰富、安全性高、免疫原性低等优势,成为干细胞治疗的理想选择之一。
然而,传统的二维(2D)培养体系存在诸多局限:难以模拟体内微环境,导致细胞形态改变,无法有效维持细胞的干性、增殖能力及免疫调节功能,且细胞产量难以满足临床需求,严重制约了hUCMSCs在银屑病治疗中的应用。如何突破这一瓶颈,提升hUCMSCs的治疗效能,成为科研团队亟待解决的关键问题。
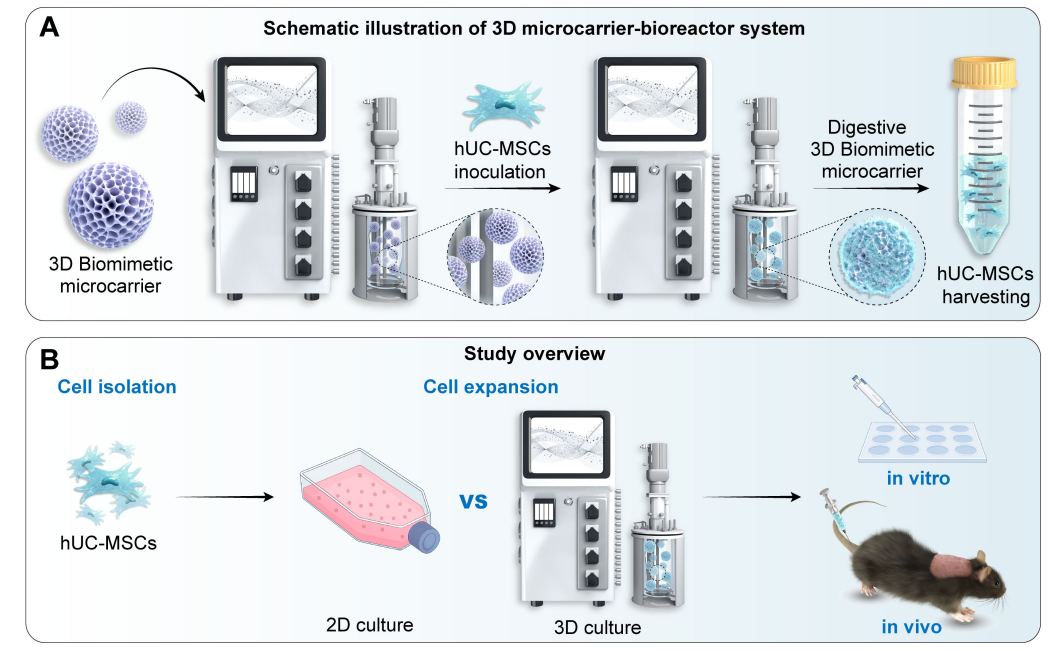
取自原文:Fig 1
研究团队通过中科睿极(海宁)生物科技有限公司DASEA® 数字化 (Digitalized)、自动化 (Automated)、规模化 (Scalable)、封闭化 (Enclosed)、活性化(Activated) 3D智能平台,采用非动物源性重组胶原微载体(CDE:F20230000567):微载体的孔隙率>90%,粒径大小可控于150-400μm之间,结合DASEA® Regenbio全自动3D细胞培养系统,为hUCMSCs提供接近体内的生长微环境,实现了干细胞规模化的三维培养扩增。随后将三维扩增细胞与常规二维培养条件下hUC-MSCs进行比较,检测其形态学、增殖能力、衰老状态、分化潜能及免疫调节特性。继而通过体外实验及咪喹莫特(IMQ)+白细胞介素23(IL-23)诱导的银屑病皮炎小鼠模型,评估了其治疗效果。
研究结果2
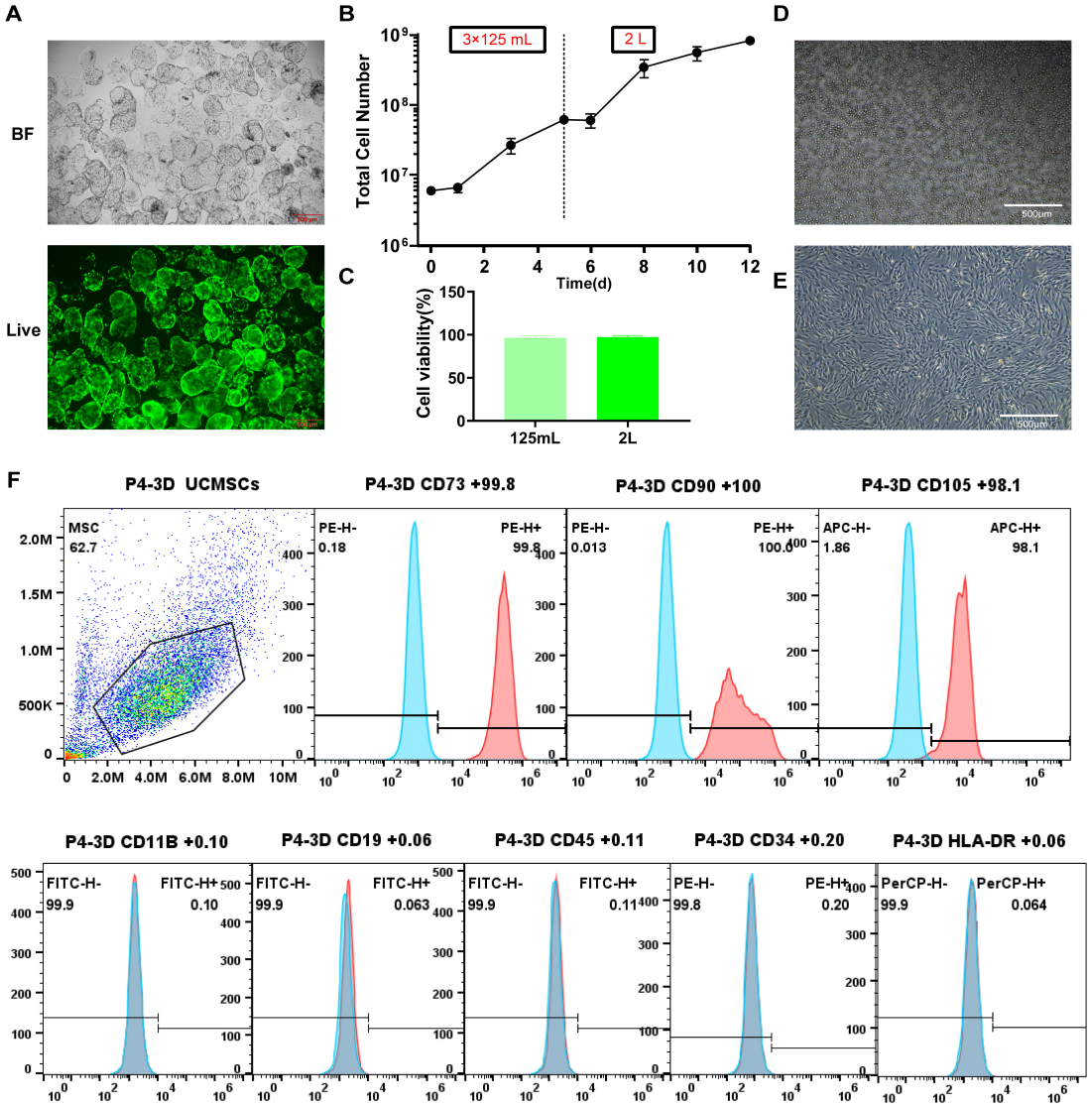
取自原文:Fig 2
首先,对收获的3D-MSCs进行了系列基础生物学属性检测。结果显示,3D仿生微载体可支持hUC-MSCs高效附着与增殖(Fig 2A);125mL和2L生物反应器收获的细胞活力均超95%,最终能获得高产量细胞(Fig 2B-C);微载体裂解后残留达标且无可见碎片(Fig 2D),3D培养的hUC-MSCs能够保持梭形成纤维细胞形态(Fig 2E)及标准抗原表型(高表达 CD73、CD90、CD105,低表达 CD11b、CD19、CD45、CD34、HLA-DR阴性标志物)(Fig 2F)。综上,3D仿生微载体培养系统在提升hUC-MSCs的附着能力和增殖效率的同时,能维持细胞的优良形态和标准表型表达。
研究结果3
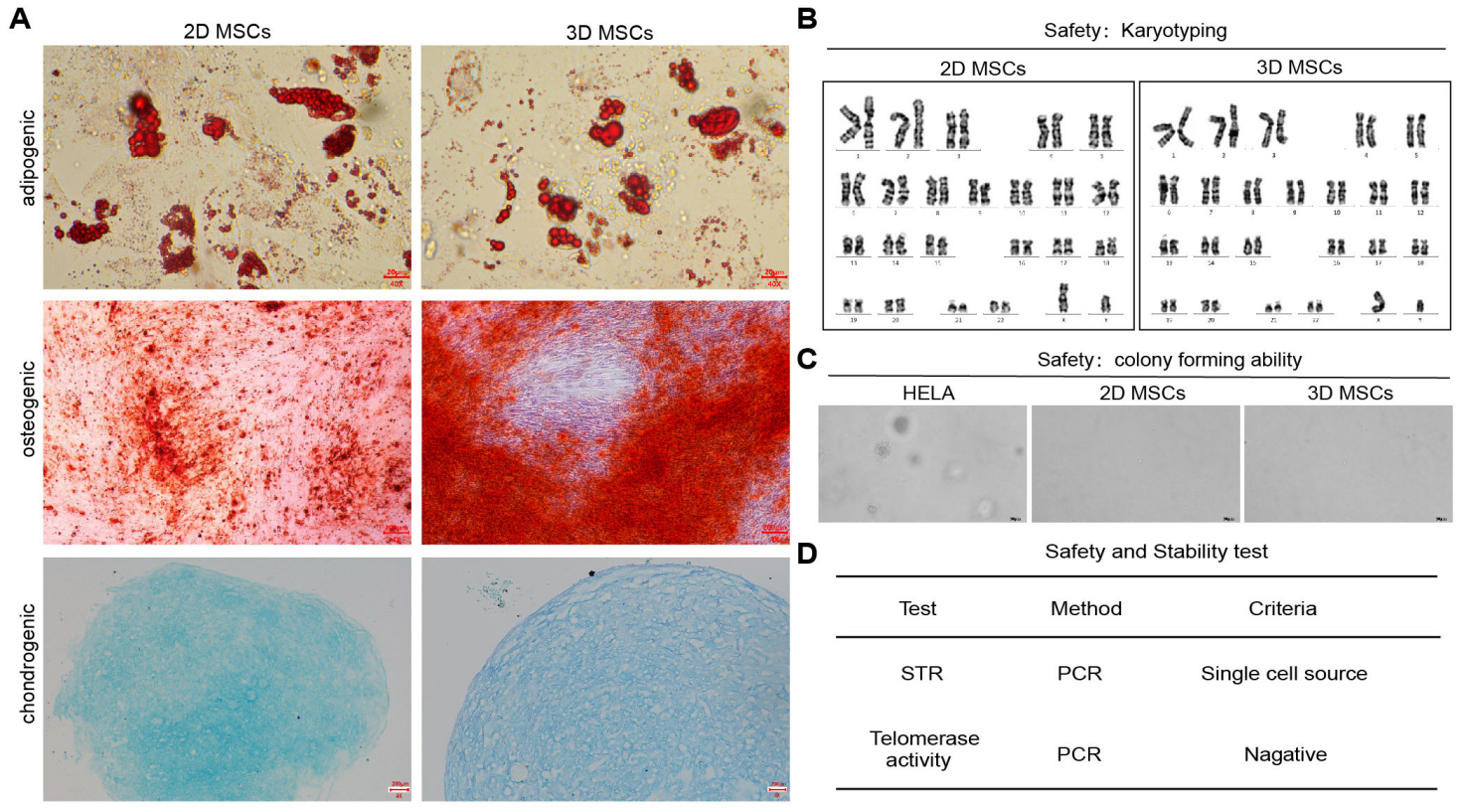
取自原文:Fig3
接着,分别评估了2D-MSCs、3D-MSCs的细胞质量和安全性。3D-MSCs仍具备向脂肪细胞、成骨细胞和软骨细胞分化的能力,分化潜能未受影响(Fig 3A)。核型分析显示,3D-MSCs的染色体结构/数量无异常,基因组保持稳定(Fig 3B)。软琼脂集落形成实验表明,3D-MSCs无克隆集落形成,且端粒酶活性检测结果为阴性,证明其无致瘤风险(Fig 3C-D)。短串联重复序列(STR)分析表明,3D-MSCs未受到其他细胞污染,细胞来源单一(Fig 3D)。 综上,3D培养条件可维持hUC-MSCs的多向分化潜能、基因组稳定性和无致瘤性,其核心质量与2D培养的细胞一致,安全性得到验证。
研究结果4
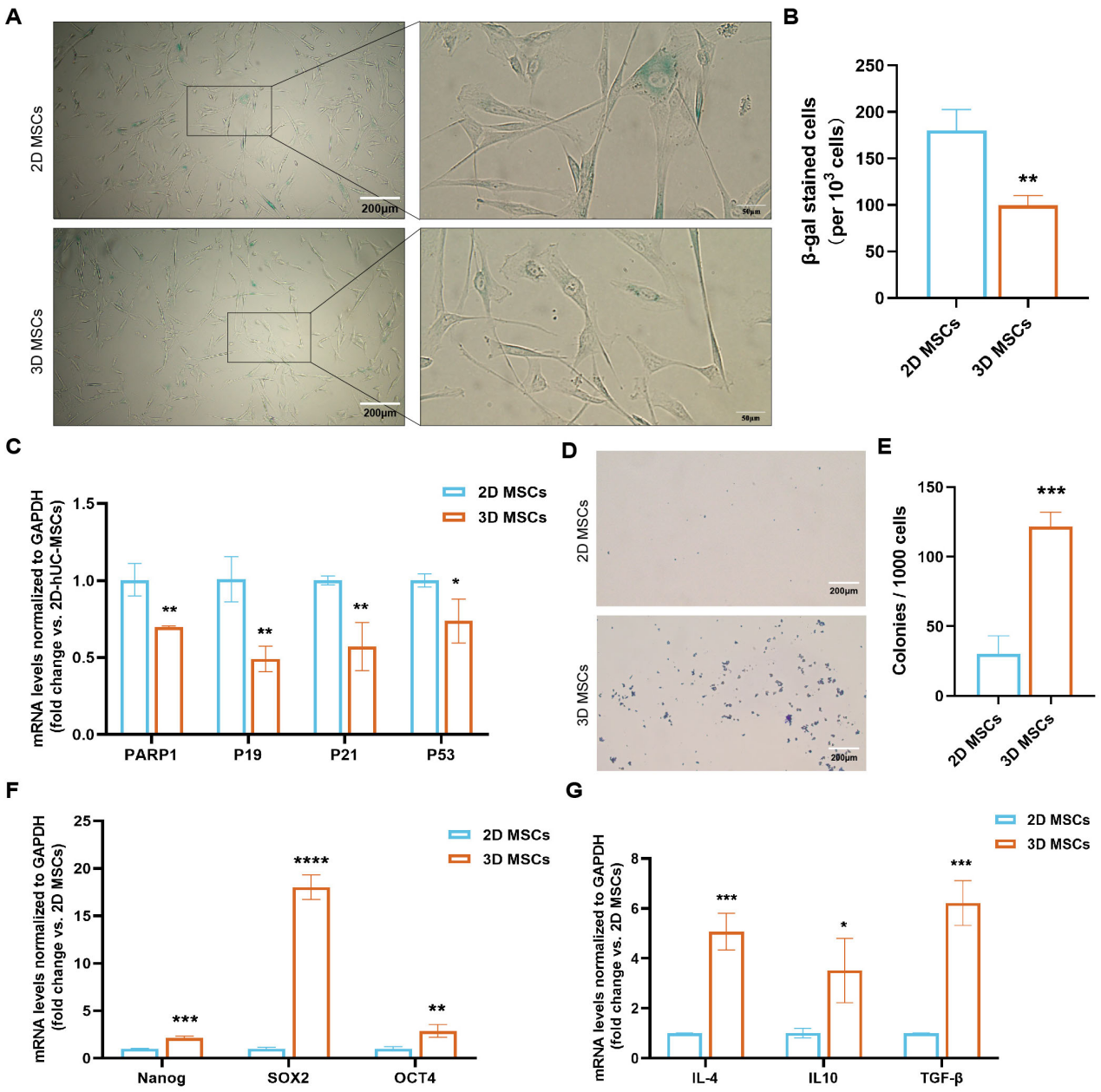
取自原文:Fig 4
继续评估2D与3D培养的hUC-MSCs在细胞衰老、活力、多能性及免疫调节因子表达方面的差异。经β-半乳糖苷酶染色分析,3D-MSCs衰老细胞占比未升高(Fig 4A-B);且衰老相关标志物 PARP1、P19、P21、P53的mRNA表达水平显著低于2D-MSCs(Fig 4C)。3D-MSCs的成纤维细胞集落形成单位(CFU-F)数量较2D-MSCs显著增加(Fig 4D-E)。RT-qPCR检测显示,3D-MSCs中多能性标志物 OCT4、SOX2、NANOG的mRNA表达水平高于2D-MSCs(Fig 4F)。3D-MSCs中免疫调节及抗炎因子 IL-4、IL-10、TGF-β的mRNA表达水平显著升高,表明其抗炎和免疫调节能力更优(Fig 4G)。综上,3D培养条件可有效减少 hUC-MSCs 的衰老,增强其增殖活力、多能性及免疫调节功能,优于传统2D培养方式。
研究结果5
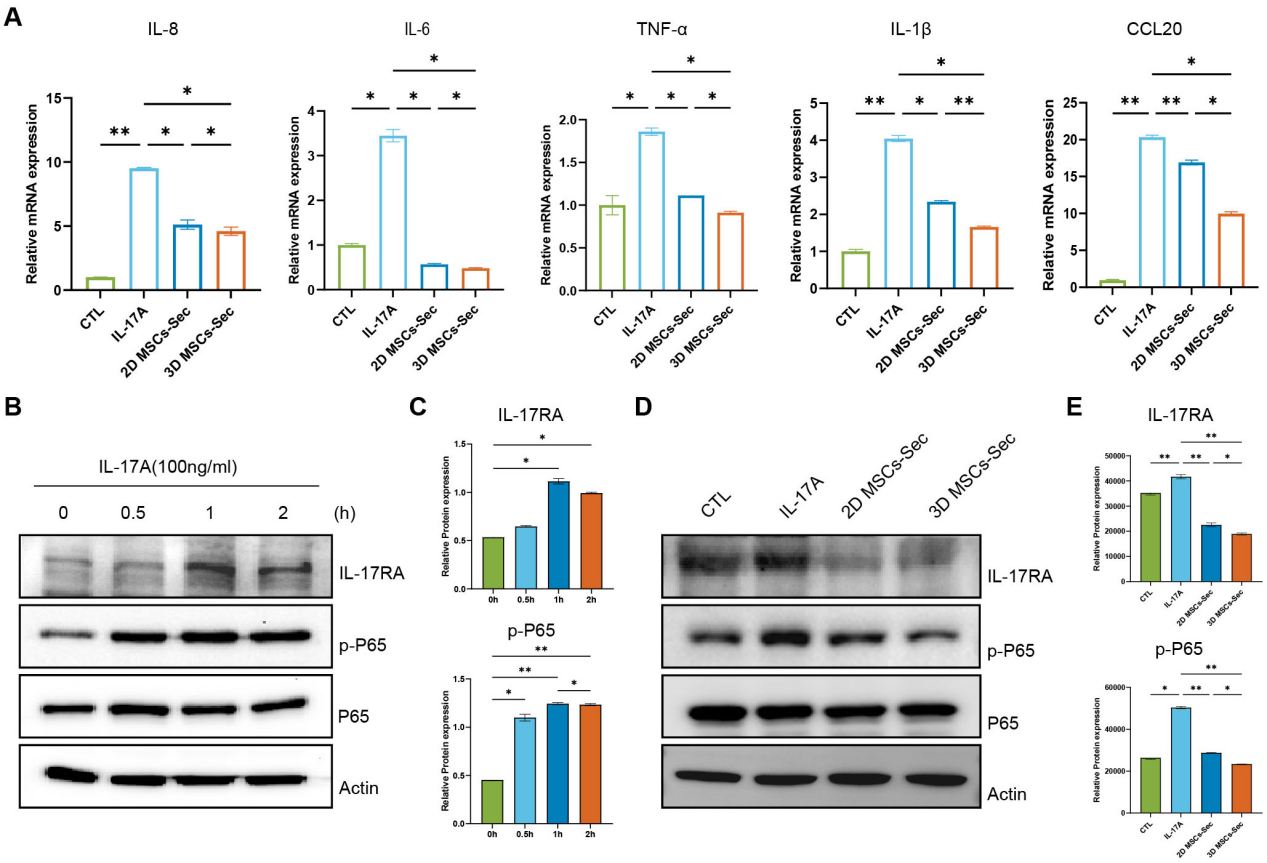
取自原文:Fig 5
接着探究了3D-MSCs上清液(3D-MSCs-Sec)在体外人永生化角质形成细胞(HaCaT)对 IL-17A激活的NF-κB信号通路的抑制作用。结果显示,3D-MSCs-Sec可显著下调HaCaT细胞中炎症因子(IL-8、IL-6、TNF-α、IL-1β及 CCL20)的mRNA表达水平(Fig 5A)。且IL-17A可时间依赖性激活角质形成细胞的IL-17RA/NF-κB通路,IL-17RA及磷酸化 P65(p-P65)蛋白的表达随刺激时间延长明显升高(Fig 5B-C)。与2D-MSCs-Sec相比,3D-MSCs-Sec能更有效地降低IL-17A刺激后HaCaT细胞中IL-17RA和p-P65的蛋白表达水平,显著抑制 NF-κB 通路的激活(Fig 5D-E)。综上,hUC-MSCs的上清液可通过抑制 IL-17RA/NF-κB信号通路缓解角质形成细胞的炎症反应,且3D培养的hUC-MSCs上清液的抑制效果优于2D培养组。
研究结果6
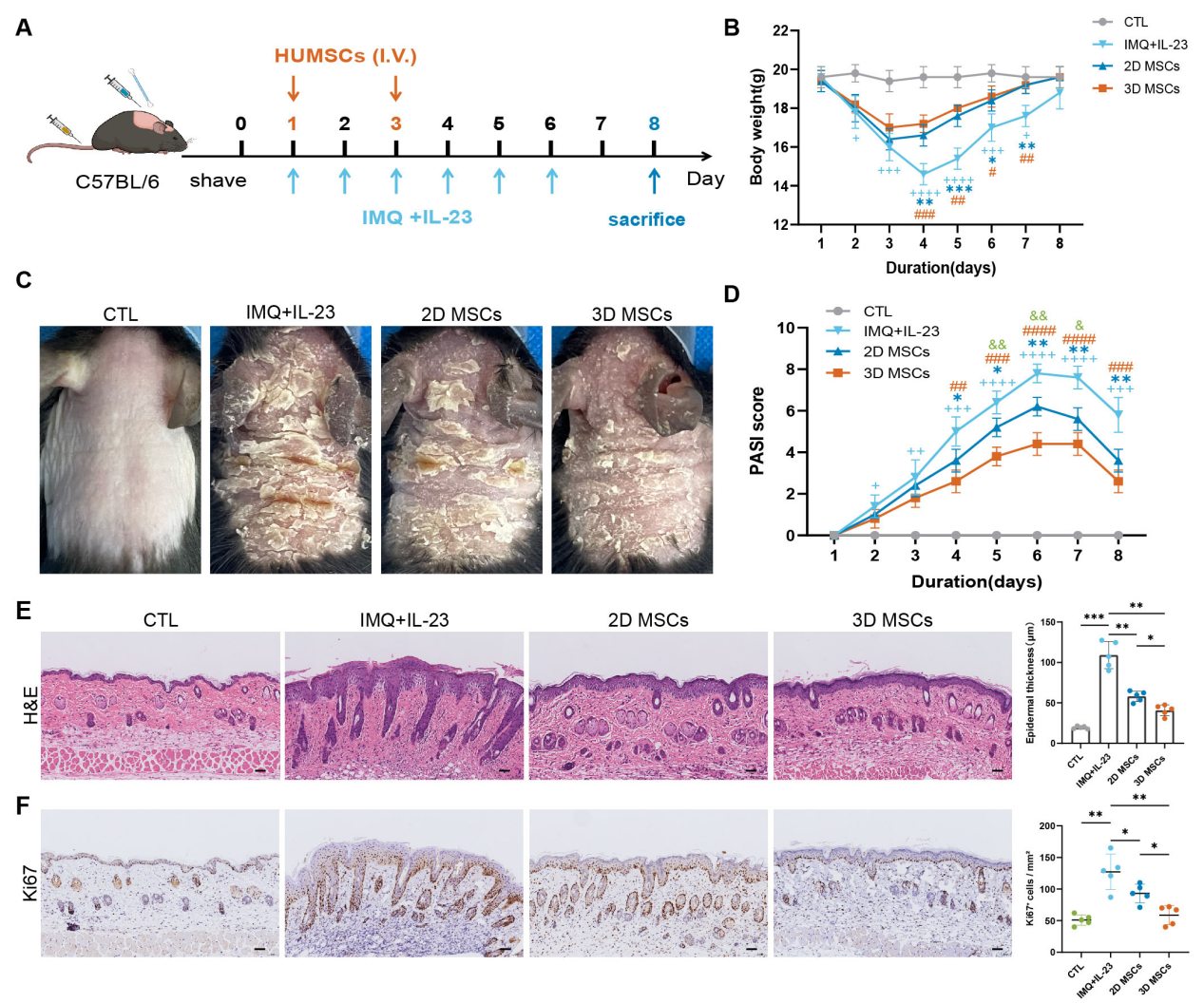
取自原文:Fig 6
将C57BL/6小鼠随机分为对照组、咪喹莫特IMQ+IL-23模型组、2D-hUC-MSCs治疗组和3D-hUC-MSCs治疗组,模型组连续7天背部涂抹咪喹莫特乳膏并皮下注射IL-23,治疗组在第1、3天尾静脉注射对应细胞(5×10⁵个cells/只),对照组给予凡士林和PBS处理,第8天处死小鼠收集样本(Fig 6A)。结果显示,在IMQ+IL-23诱导的银屑病小鼠模型中,3D-hUC-MSCs治疗组相较2D-hUC-MSCs组和模型组,能更显著缓解小鼠体重下降,改善背部皮肤红斑、脱屑等表型异常,降低PASI(银屑病面积和严重程度指数)评分(Fig 6B-D);同时可有效减薄增厚的表皮,减少皮肤炎症细胞浸润,抑制增殖细胞标志物Ki67阳性细胞的异常增殖,整体治疗效果和病理改善程度均优于2D-hUC-MSCs治疗组(Fig 6E-F),证实3D-hUC-MSCs在体内对银屑病样炎症的缓解作用更显著。
研究结果7
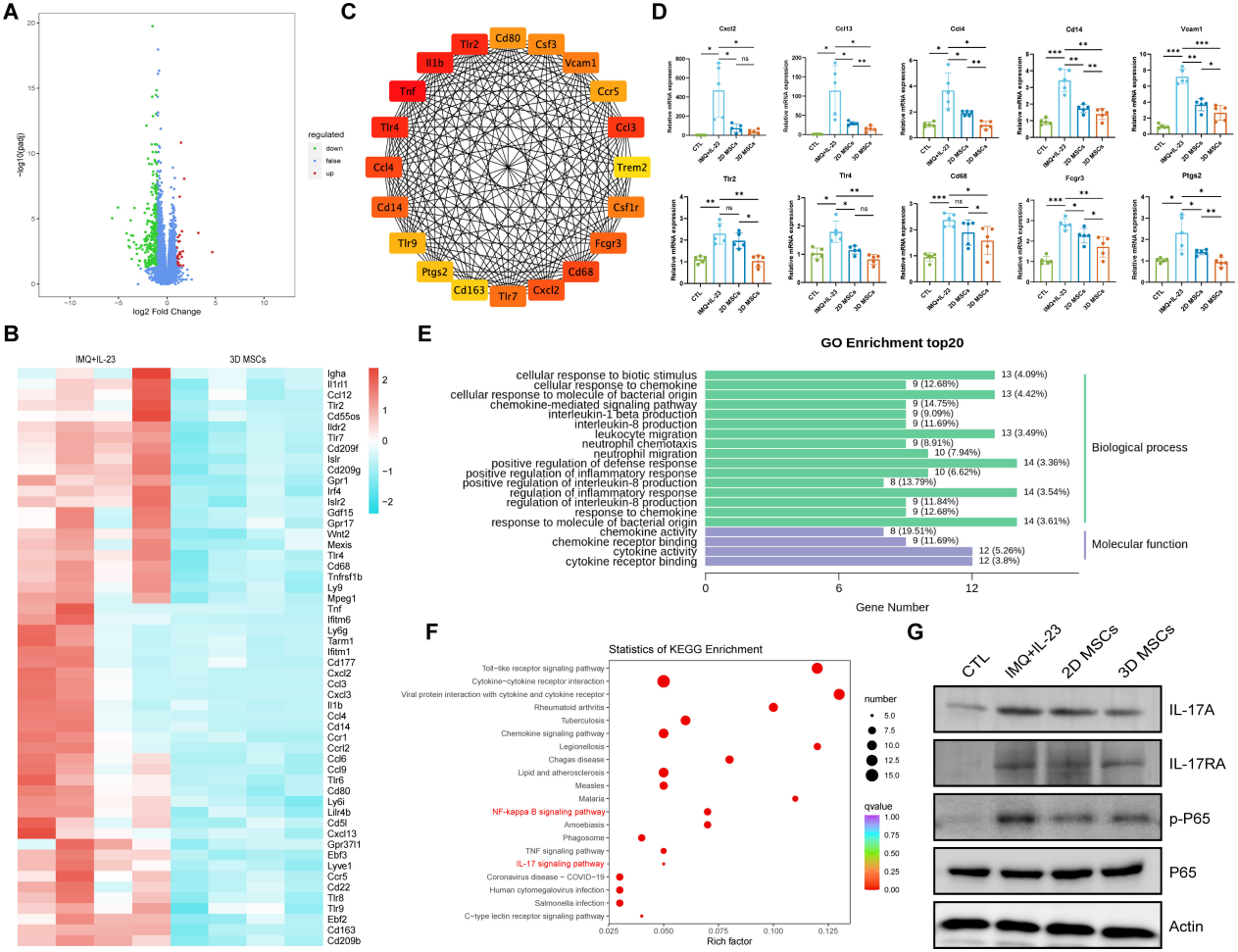
取自原文:Fig 7
通过RNA测序(RNA-seq)探究3D-hUC-MSCs调控银屑病样炎症的分子机制。相较于IMQ+IL-23模型组,3D-hUC-MSCs治疗组有 324个基因表达显著改变(291个下调、33个上调),且下调基因多与炎症相关(Fig 7AB);蛋白质 - 蛋白质相互作用(PPI)网络分析筛选出20个下调核心基因,这些基因可能通过协同作用调控银屑病病理过程中的炎症反应与免疫调节(Fig 7C);RT-qPCR验证了排名前10的关键下调基因,进一步证实其在3D-hUC-MSCs治疗中的重要性(Fig 7D)。功能富集分析表明这些差异基因参与信号转导、先天免疫反应等过程,且富集于NF-κB、IL-17等关键炎症通路(Fig 7EF);Western blot验证显示,3D-hUC-MSCs可显著降低小鼠皮肤组织IL-17A、IL-17RA及 p-P65的蛋白表达(Fig 7G),证实IL-17/NF-κB信号通路是其调控银屑病样炎症的核心靶点,3D-hUC-MSCs通过下调炎症相关基因、抑制该通路激活发挥治疗作用。
研究结果8
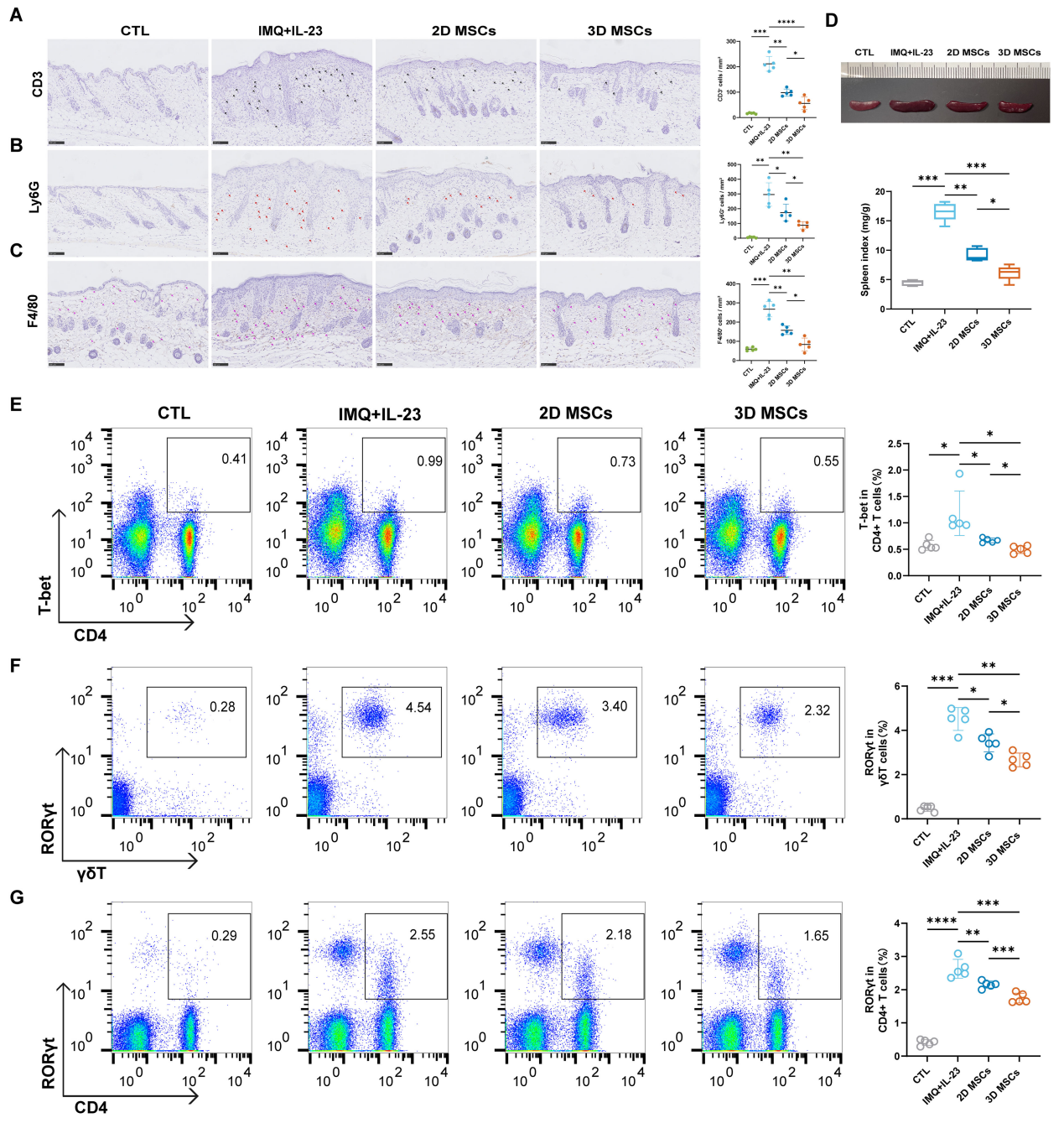
取自原文:Fig 8
为探究3D-hUC-MSCs缓解银屑病的作用机制,在第8天对小鼠皮肤微环境进行了评估。免疫组化分析显示,3D-hUC-MSCs能显著减少 IMQ+IL-23诱导的银屑病模型小鼠皮肤中 CD3+T细胞、Ly6G+中性粒细胞及 F4/80+巨噬细胞的浸润(Fig 8A-C)。脾脏指数(衡量脾脏重量与体重的比值,作为炎症严重程度的指标)在3D-hUC-MSCs处理的小鼠中降低(Fig 8D)。流式细胞术分析显示,与模型组相比,3D-hUC-MSCs治疗组小鼠淋巴结中T-bet+/CD4+ T细胞、RORγT+/CD4+ T细胞及 RORγT+/γδT细胞的百分比和绝对数量均显著减少,表明其可抑制 T细胞增殖并调控 Th1、Th17细胞应答(Fig 8E-G)。
研究结果9
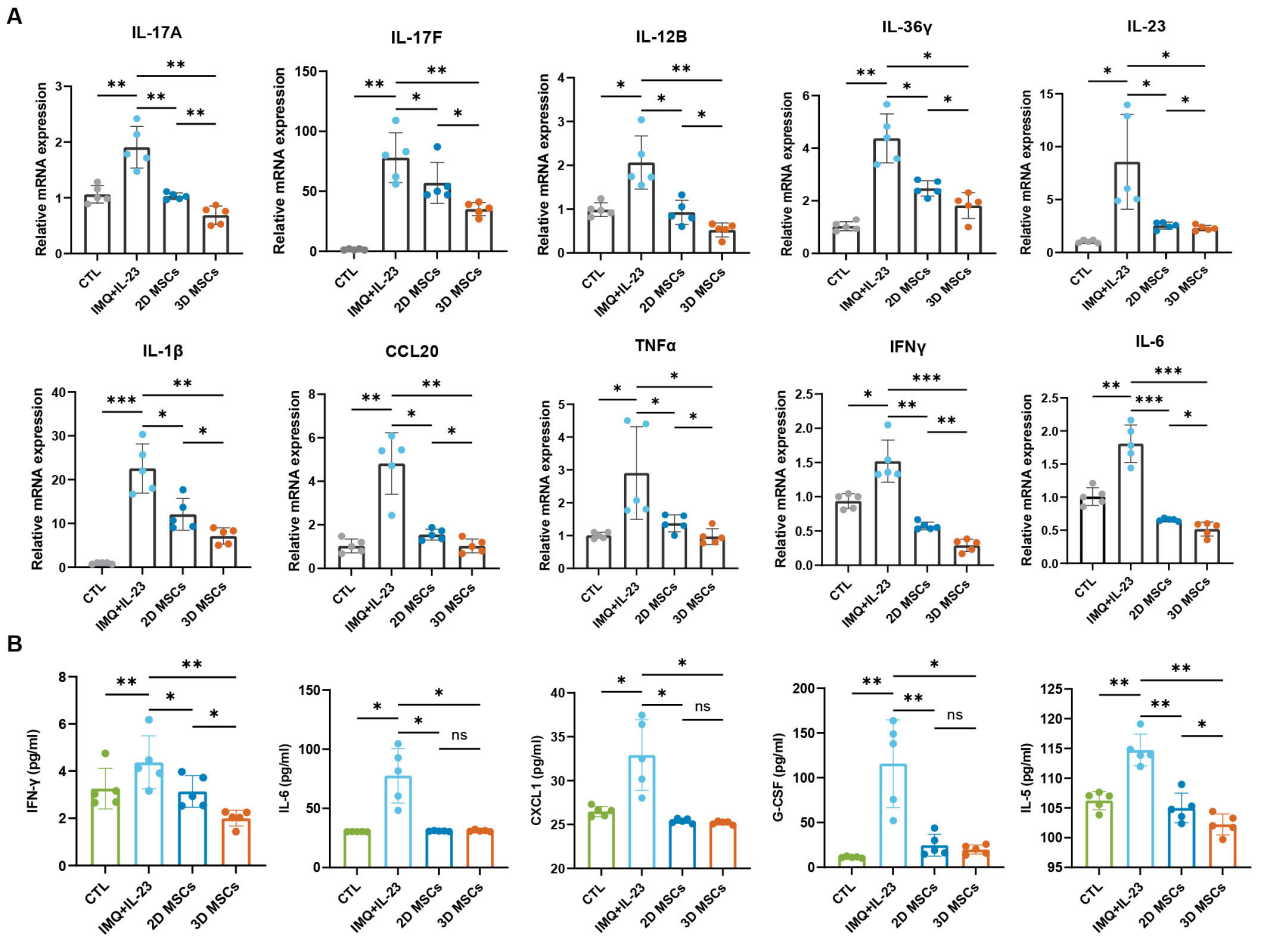
取自原文:Fig 9
RT-qPCR 检测显示,与 IMQ+IL-23模型组相比,3D-hUC-MSCs治疗组小鼠皮肤组织中 Il-17A、Il-17F、IL-12B、IL-23、IL-36g、IFN-γ、IL-6、TNF-α、IL-1β 及CCL20等基因的mRNA表达水平显著降低(Fig 9A)。ELISA检测证实,3D-hUC-MSCs治疗后,小鼠血清中IFN-γ、IL-6、CXCL1、G-CSF 及IL-5等促炎因子的表达量明显下降,与皮肤组织中细胞因子的下调趋势一致(Fig 9B)。
研究结论
该研究证实,基于3D仿生微载体的培养系统可显著提升hUC-MSCs的增殖能力、干细胞特性及免疫调节功能,且维持其基因组稳定性与多向分化潜能,通过抑制 IL-17/NF-κB 信号通路、减少免疫细胞浸润及促炎因子产生,在体内外对银屑病样炎症的治疗效果优于传统 2D 培养的 hUC-MSCs,为自身免疫性疾病治疗、再生医学等领域提供了高效的 MSC制备策略。
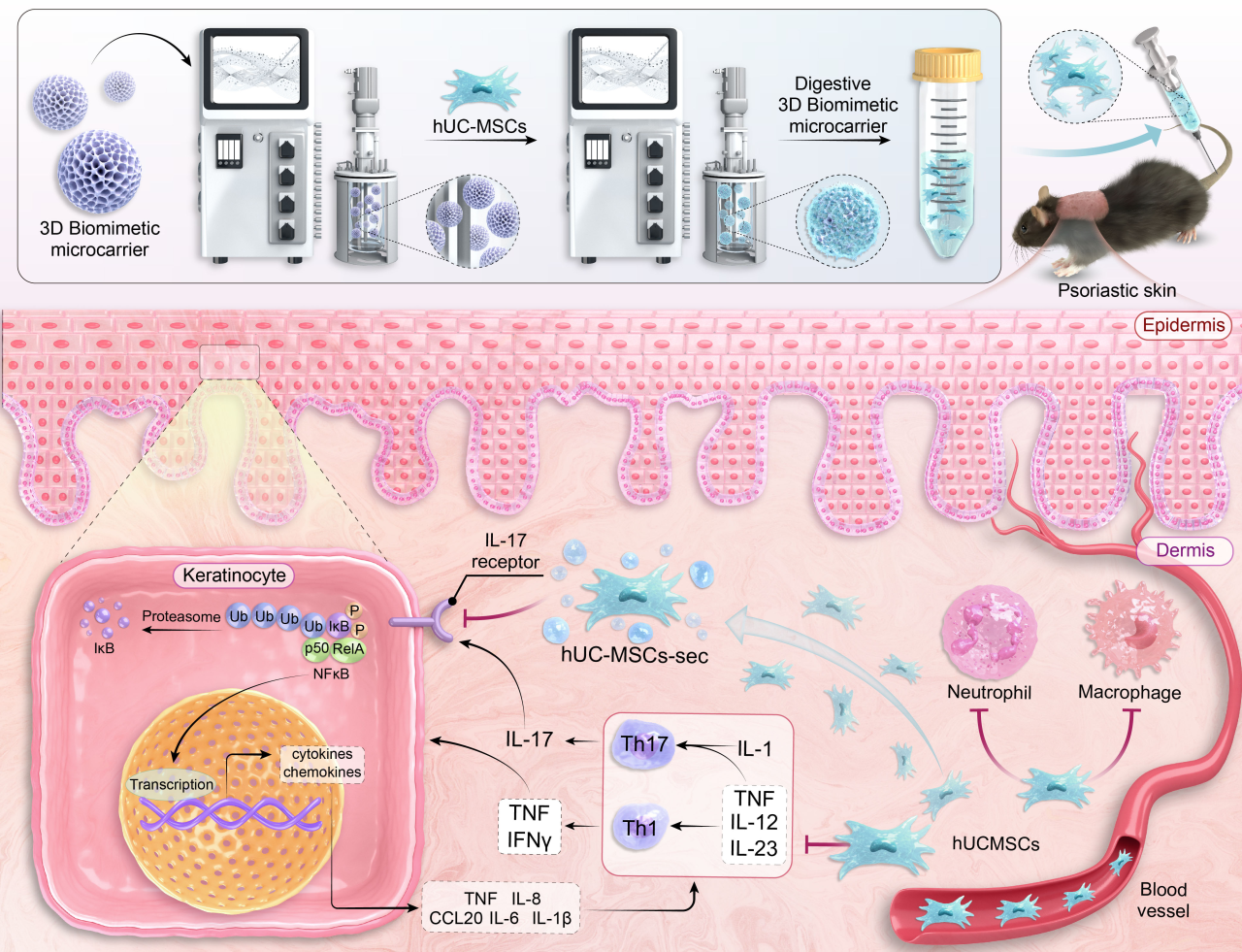
取自原文:Fig 10
3D 智能平台研究技术支持
本项研究中干细胞三维培养制备技术由中科睿极(海宁)生物科技有限公司提供支持,包括DASEA®生物智造平台的MSCs、DASEA® Ultramedia® Pro培养基、DASEA® Regencarrier® 仿生型微载体、裂解液、DASEA® Regenbio 全自动3D细胞培养系统等。
原文链接:https://www.frontiersin.org/articles/10.3389/fimmu.2026.1687424
最热新闻

2026-03-09

2025-12-23

2025-12-19

2025-11-20

2025-09-01

2025-06-25

2025-06-21

2025-05-06

2025-01-13

2025-01-09

2025-01-04

2024-08-23

2024-07-18

2024-06-22

2024-06-17

2024-05-28

2024-05-27

2024-02-05

2024-01-03

2024-06-21
相关标签






